Гомоцистеин и UPR — различия между версиями
Alexander (обсуждение | вклад) |
м |
||
| (не показана 31 промежуточная версия 2 участников) | |||
| Строка 1: | Строка 1: | ||
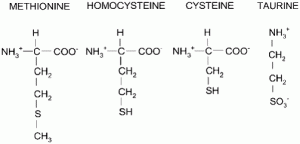
| − | '''Гомоцистеин''' (SCH2CH2CH(NH2)CO2H) | + | '''Гомоцистеин''' [[Изображение:SulfurAA.gif|Серосодержащие аминокислоты |thumb|right]](Hcy, формула SCH2CH2CH(NH2)CO2H) — аминокислота, участвующая в метаболизме живых организмов, наряду с цистеином, метионином и, условно, таурином, относящаяся к серосодержащим. |
| − | Интерес к изучению эффектов данной аминокислоты патофизиологами связан с широким распространением патологического состояния | + | Интерес к изучению эффектов данной аминокислоты патофизиологами связан с широким распространением патологического состояния — гипергомоцистеинемия . Это состояние характеризуется повышением содержания в плазме Hcy свыше 12 мкмоль/л, причиной которого могут служить мутации ферментов метаболизма гомоцистеина, недостаточность его кофакторов (то есть витаминов — B6, B12, фолиевой кислоты), лекарственные средства, нарушение выделительной функции организма. |
| − | Последствия серьезны: рост риска атеросклероза (60-80%, в зависимости от группы изучения, при росте концентрации на 5 мкмоль/л), риск болезни Альцгеймера, нарушение фетоплацентарного (плод | + | |
| + | Последствия гипергомоцистеинемии серьезны: рост риска атеросклероза (60-80 %, в зависимости от группы изучения, при росте концентрации на 5 мкмоль/л), риск болезни Альцгеймера, нарушение фетоплацентарного (плод — плацента) кровообращения при беременности, ухудшение прогноза по сосудистым осложнениям сахарного диабета. При этом имеет место снижение на 25 % риска инсульта при коррекции недостатка кофакторов обмена Hcy в качестве бонуса. | ||
== Метаболизм гомоцистеина == | == Метаболизм гомоцистеина == | ||
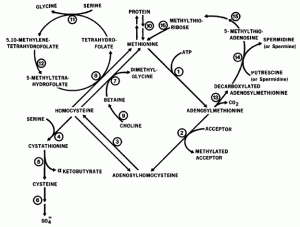
| − | ---- | + | [[Изображение:MethabHcy.gif|Метаболизм гомоцистеина.|thumb|right]]Обмен Hcy в организме тесно связан с обменом метионина (Met) и его метаболически-активной «модификации» аденозилметионина (AdoMet). Кроме участия в составе аминокислот, практически всё участие метионина в обмене веществ проходит через образование AdoMet. Основными реакциями, в которых участвует AdoMet, являются реакции трансметилирования (переноса метильной группы), значение которых в жизни клетки трудно переоценить: это и синтез множества БАВ (холин, адреналин, креатин), и [[rupedia:метилирование_ДНК|метилирование ДНК]] (один из важнейших механизмов «глобальной» [[rupedia:Эпигенетика|эпигенетической]] регуляции генной активности). Трансметилирование осуществляет большая группа ферментов — трансметилаз. |
| + | |||
| + | Перенос метильной группы с AdoMet ведет к образованию аденозилгомоцистеина (AdoHcy), причем накопление этого продукта реакции трансметилирования ведет к ингибированию самой реакции. Это требует немедленного дальнейшего превращения AdoHcy, что реализуется аденозилгомоцистеиназой и связыванием с белком. Образующийся Hcy также должен удаляться из сферы реакции: наряду с AdoHcy он связывается с внутриклеточными белками и экспортируется из клетки, связываясь с белками плазмы, и выводясь, в результате, почками. Hcy, в отличие от AdoHcy, может еще и метаболизироваться тканями организма. Тут существует три реакции: две реметилирования (возврат перенесенных при трансметилировании метильных групп) в Met, одна транссульфирования (перенос сульфатных групп) в цистеин. | ||
| + | * Первый тип ремитилирования осуществляется переносом метильной группы с бетаина с помощью бетаин-гомоцистеин метилтрансферазы (тут задействован и витамин B6). | ||
| + | * Второй тип ремитилирования осуществляется переносом метильной группы с 5-метилтетрагидрофолата c помощью метилфолат-гомоцистеин метилтрансферазы (здесь требуется участие витамина B12). Причем, донор метильной группы — 5-метилтетрагидрофолат, образуется с помощью фермента метилтетрагидрофолатредуктазы (MTHFR). | ||
| + | |||
| + | Транссульфирование с точки зрения патофизиологии нам менее интересно. Важно, что нарушение работы MTHFR и бетаин-гомоцистеин метилтрансферазы в следствии, например, мутаций и ведет к той самой гипергомоцистеинемии. | ||
| + | |||
| + | == Эффекты гомоцистеина в тканях и культурах клеток == | ||
| + | |||
| + | Показано что в тканях организма повышенное содержание гомоцистеина ведет к: | ||
| + | * Гибели клеток эндотелия (клеток, выстилающих сосуды изнутри) | ||
| + | * Пролиферации клеток гладкомышечного слоя стенки сосудов (ведет к сужению просвета сосуда, нарушению эластических свойств стенки) | ||
| + | * Смещению соотношения фракций липопротеидов в сторону «плохих», содержащих холестерин липопротеидов низкой плотности (ЛПНП) | ||
| + | * Индукции аутоиммунного ответа (то есть аутоагрессии иммунной системы на свои ткани) | ||
| + | * Образованию тромбов в сосудах | ||
| + | |||
| + | Для клеточных культур (то есть однородных клеток одной ткани, адаптированных к росту в специальных фляжках-"матрасах") показаны разнородные эффекты для разных культур, в целом совпадающие с тем что имеет место в тканях. | ||
| + | |||
| + | [[Категория:Биоинформатика]] | ||
Текущая версия на 20:09, 24 марта 2010
Гомоцистеин (Hcy, формула SCH2CH2CH(NH2)CO2H) — аминокислота, участвующая в метаболизме живых организмов, наряду с цистеином, метионином и, условно, таурином, относящаяся к серосодержащим.Интерес к изучению эффектов данной аминокислоты патофизиологами связан с широким распространением патологического состояния — гипергомоцистеинемия . Это состояние характеризуется повышением содержания в плазме Hcy свыше 12 мкмоль/л, причиной которого могут служить мутации ферментов метаболизма гомоцистеина, недостаточность его кофакторов (то есть витаминов — B6, B12, фолиевой кислоты), лекарственные средства, нарушение выделительной функции организма.
Последствия гипергомоцистеинемии серьезны: рост риска атеросклероза (60-80 %, в зависимости от группы изучения, при росте концентрации на 5 мкмоль/л), риск болезни Альцгеймера, нарушение фетоплацентарного (плод — плацента) кровообращения при беременности, ухудшение прогноза по сосудистым осложнениям сахарного диабета. При этом имеет место снижение на 25 % риска инсульта при коррекции недостатка кофакторов обмена Hcy в качестве бонуса.
Метаболизм гомоцистеина
Обмен Hcy в организме тесно связан с обменом метионина (Met) и его метаболически-активной «модификации» аденозилметионина (AdoMet). Кроме участия в составе аминокислот, практически всё участие метионина в обмене веществ проходит через образование AdoMet. Основными реакциями, в которых участвует AdoMet, являются реакции трансметилирования (переноса метильной группы), значение которых в жизни клетки трудно переоценить: это и синтез множества БАВ (холин, адреналин, креатин), и метилирование ДНК (один из важнейших механизмов «глобальной» эпигенетической регуляции генной активности). Трансметилирование осуществляет большая группа ферментов — трансметилаз.Перенос метильной группы с AdoMet ведет к образованию аденозилгомоцистеина (AdoHcy), причем накопление этого продукта реакции трансметилирования ведет к ингибированию самой реакции. Это требует немедленного дальнейшего превращения AdoHcy, что реализуется аденозилгомоцистеиназой и связыванием с белком. Образующийся Hcy также должен удаляться из сферы реакции: наряду с AdoHcy он связывается с внутриклеточными белками и экспортируется из клетки, связываясь с белками плазмы, и выводясь, в результате, почками. Hcy, в отличие от AdoHcy, может еще и метаболизироваться тканями организма. Тут существует три реакции: две реметилирования (возврат перенесенных при трансметилировании метильных групп) в Met, одна транссульфирования (перенос сульфатных групп) в цистеин.
- Первый тип ремитилирования осуществляется переносом метильной группы с бетаина с помощью бетаин-гомоцистеин метилтрансферазы (тут задействован и витамин B6).
- Второй тип ремитилирования осуществляется переносом метильной группы с 5-метилтетрагидрофолата c помощью метилфолат-гомоцистеин метилтрансферазы (здесь требуется участие витамина B12). Причем, донор метильной группы — 5-метилтетрагидрофолат, образуется с помощью фермента метилтетрагидрофолатредуктазы (MTHFR).
Транссульфирование с точки зрения патофизиологии нам менее интересно. Важно, что нарушение работы MTHFR и бетаин-гомоцистеин метилтрансферазы в следствии, например, мутаций и ведет к той самой гипергомоцистеинемии.
Эффекты гомоцистеина в тканях и культурах клеток
Показано что в тканях организма повышенное содержание гомоцистеина ведет к:
- Гибели клеток эндотелия (клеток, выстилающих сосуды изнутри)
- Пролиферации клеток гладкомышечного слоя стенки сосудов (ведет к сужению просвета сосуда, нарушению эластических свойств стенки)
- Смещению соотношения фракций липопротеидов в сторону «плохих», содержащих холестерин липопротеидов низкой плотности (ЛПНП)
- Индукции аутоиммунного ответа (то есть аутоагрессии иммунной системы на свои ткани)
- Образованию тромбов в сосудах
Для клеточных культур (то есть однородных клеток одной ткани, адаптированных к росту в специальных фляжках-"матрасах") показаны разнородные эффекты для разных культур, в целом совпадающие с тем что имеет место в тканях.